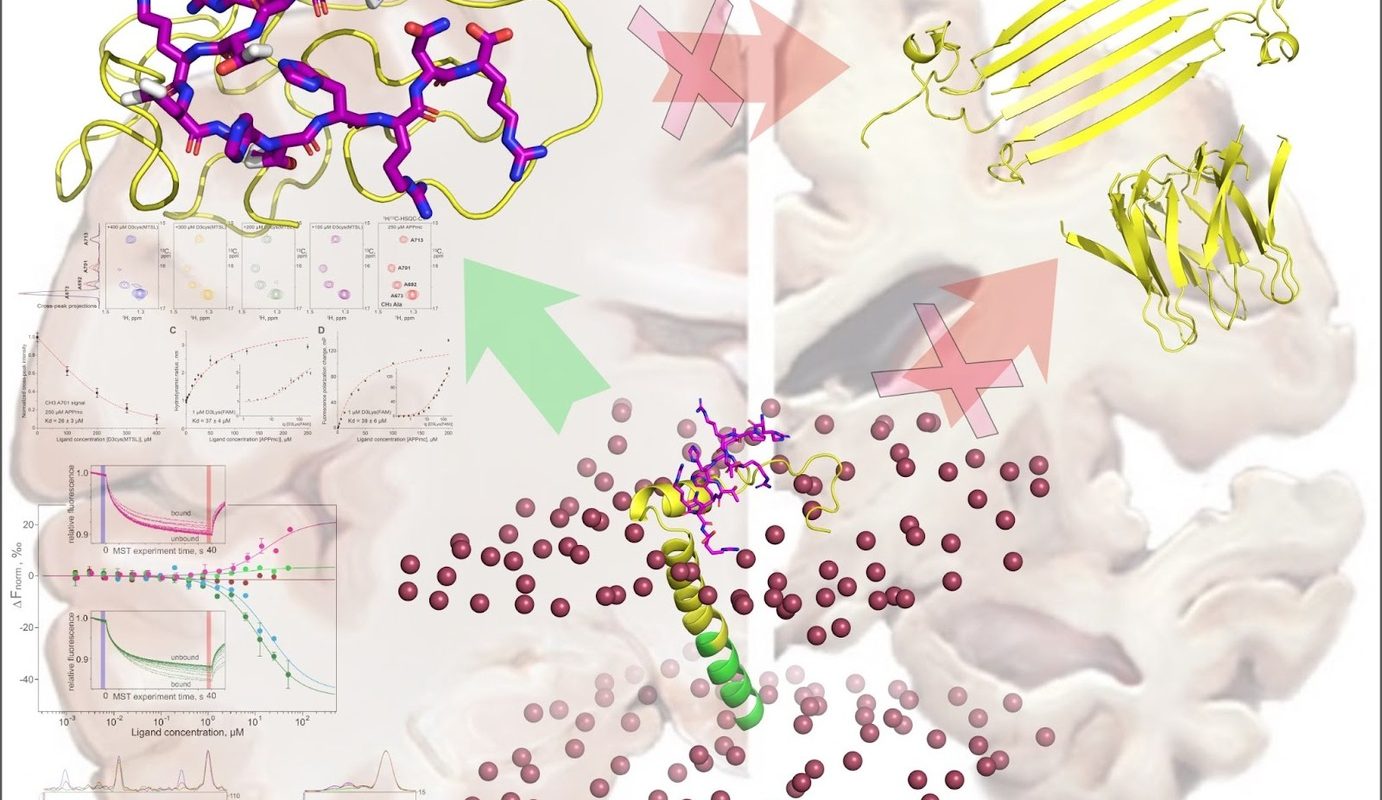
Ученые Центра исследований молекулярных механизмов старения и возрастных заболеваний МФТИ в сотрудничестве с коллегами из Института биоорганической химии им. академиков М. М. Шемякина и Ю. А. Овчинникова РАН и Исследовательским центром города Юлиха провели экспериментальное исследование перспективного лекарственного средства от нейродегенерации. Результаты исследований, поддержанных РНФ (20-64-46027), опубликованы в Journal of Medicinal Chemistry и являются существенным шагом к решению застарелой проблемы всего человечества — лечению болезни Альцгеймера. Процесс старения включает в себя различные возрастные нейродегенеративные заболевания, нарушающие сложную сеть метаболических и сигнальных путей. Болезнь Альцгеймера — самый распространенный в мире вид нейродегенеративного заболевания, которым ежегодно заболевает несколько миллионов человек, причем с возрастом вероятность развития этого вида деменции возрастает многократно. Сегодня уже более 50 миллионов человек во всем мире страдают от нейродегенерации, вызванной болезнью Альцгеймера, и ожидается, что из-за увеличения продолжительности жизни к 2050 году это число увеличится втрое. Прошло уже 110 лет с тех пор, как болезнь была впервые описана Алоисом Альцгеймером как форма прогрессирующего нейродегенеративного и поведенческого расстройства. Несмотря на прогресс в науке и медицине, на обширные исследования и огромное количество информации, полученной по различным аспектам болезни, ее причины и молекулярные механизмы остаются в значительной степени неизвестными и по-прежнему не существует эффективного метода лечения и профилактики. Сейчас мы знаем, что клинические проявления болезни Альцгеймера объясняются избирательной дегенерацией нейронов в участках коры головного мозга, ответственных за когнитивное восприятие и память. Известно, что в патогенезе болезни Альцгеймера задействованы различные пептиды и белки, в том числе амилоидогенные: прежде всего, бета-амилоидный пептид (Aβ), а также взаимодействующие с ним Тау-белок и прионный белок PrP. Вне нервных клеток, в местах контакта нейронов, накапливается пептид Aβ, который собирается в протяженные упорядоченные структуры — фибриллы, формирующие так называемые амилоидные бляшки. В настоящий момент предложенные методы лечения основаны на разрушении внеклеточных отложений Aβ. Но это может привести к образованию гораздо более опасных малых сгруппированных вместе молекул пептида β-амилоида (олигомеров Aß), способных воздействовать на функцию белков, мембранных рецепторов и каналов, а также на нормальную работу внутриклеточных органелл, приводя к угнетению нейронов и клеточной смерти. Биологическая роль пептида β-амилоида (Aβ) в норме (не при болезни) в значительной степени неизвестна. Тем не менее очень близкие формы пептида β-амилоида, отличающиеся на один или несколько аминокислотных остатков (изоформы Aβ) различной длины встречаются у людей независимо от возраста и наличия проявлений болезни. Пептиды Aβ могут играть роль в сигнальных путях в головном мозге и, вероятно, имеют нейропротекторные свойства при низких концентрациях. Все изоформы пептидов Aβ склонны к олигомеризации, и именно олигомеры играют решающую роль в патогенезе болезни Альцгеймера, оказывая токсическое действие на нейроны и их органеллы. Поэтому профессором Дитером Вильбольдом был разработан так называемый D-энантиомерный пептид D3 и его производные для разборки и разрушения цитотоксических малых олигомеров Aβ. На данный момент одно из D3-подобных соединений находится в фазе II клинических испытаний. В результате плодотворного многолетнего сотрудничества между МФТИ и Исследовательским центром г. Юлиха (Forschungszentrum Jülich, FZJ) исследователи выяснили как происходит взаимодействие пептидов на молекулярном уровне. Оказалось, что пептид D3, стабилизирующий мономер Aβ, динамически взаимодействует с прилегающей к мембране областью мембранного белка предшественника Aβ — CTFβ. Эдуард Бочаров, ведущий исследователь, рассказал: «Мы использовали структурные данные высокого разрешения, экспериментально полученные с помощью ЯМР, как граничные условия для молекулярного моделирования. Исследование показало, что D3 нацелен на амилоидогенную область Aβ. Мы предполагаем, что тем самым он подавляет ранние стадии приобретения пептидом Aβ β-конформаций, характерных для малых токсичных олигомеров». chwitz) и ингибированием образования токсичных олигомеров Aβ (в правой верхней части рисунка). Рисунок авторов статьиСовременные методы позволяют изучать неупорядоченные белки (intrinsically disordered protein, IDP), но при этом некоторые эксперименты были проведены на грани чувствительности приборов. Например, сбор сигнала в экспериментах ЯМР (метод ядерного магнитного резонанса) занимал до трех дней. Эксперименты по определению константы диссоциации IDP-IDP комплекса заняли несколько месяцев, и были использованы все доступные команде методы. Иван Охрименко, заместитель заведующего лабораторией старения и возрастных нейродегенеративных заболеваний МФТИ, добавил: «Важно, что D3 и Aβ являются неупорядоченными белками. При взаимодействии D3 и Aβ образуется подвижный, но устойчивый IDP-IDP комплекс, в котором конформации обоих полипептидов постоянно изменяются с изменением паттерна их межмолекулярных контактов». В результате проведенных исследований впервые была экспериментально получена атомарная структура D-пептида, представителя нового перспективного класса лекарственных средств, в комплексе с прекурсором Aβ. Детальное понимание структурной динамики неупорядоченных белков позволяет разработать лекарственные средства для лечения и профилактики болезни Альцгеймера.